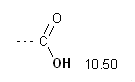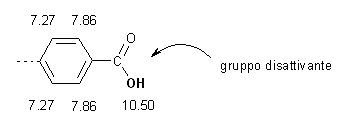|
Pianeta Chimica.it Responsabile: Prof. Mauro Tonellato |
PROBLEMA NMR N°2 |
||||||||||||||||
|
|
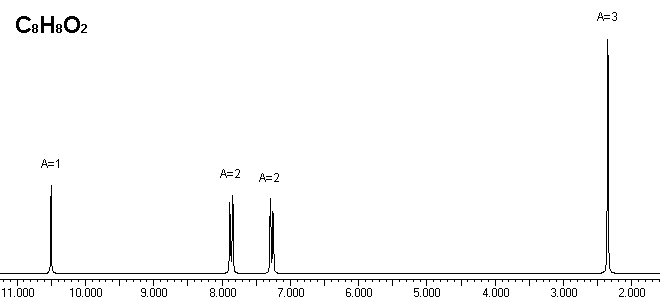
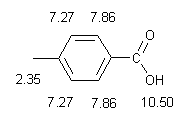
Cominciamo l'analisi dal lato sinistro dello spettro, dove vediamo il singoletto di area 1 a 10.50 ppm tipico dell'idrogeno acido di un carbossile.
Continuando l'analisi verso destra incontriamo i due doppietti di area 2 a 7.86 e 7.27 ppm tipici di un anello benzenico para disostituito. Infatti, avendo area 2, ciascun picco è dovuto a una coppia di idrogeni identici, inoltre, essendo doppietti, ogni idrogeno ha un idrogeno vicino.
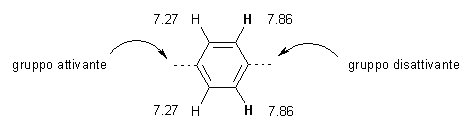
Dall'assorbimento a frequenze particolarmente
alte dei due idrogeni che risuonano a 7.86 ppm, deduciamo che
lì deve esserci un sostituente molto elettron attrattore
(un gruppo disattivante nelle reazioni di sostituzione elettrofila
aromatica). Infatti, la presenza di un gruppo elettron attrattore impoverisce
l'anello di elettroni e quindi gli idrogeni vicini vengono deschermati,
sentono un campo magnetico più intenso e risuonano a frequenze
maggiori rispetto ai 7.34 ppm del benzene.
Il sostituente che si trova dalla
parte opposta dell'anello è un gruppo debolmente attivante, infatti
gli idrogeni dell'anello assorbono a 7.27 ppm.
La molecola è quindi acido 4-metilbenzoico
|
||||||||||||||||
|
|
|||||||||||||||||
|
|
|||||||||||||||||
|
email: info@pianetachimica.it
|
|||||||||||||||||