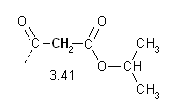|
Pianeta Chimica.it Responsabile: Prof. Mauro Tonellato |
PROBLEMA NMR N°40 |
||||||||||||||||
|
|
Iniziamo a leggere lo
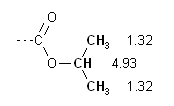
spettro da sinistra e consideriamo l'eptetto di area 1 a 4.93 ppm.
E' dovuto ad un CH legato all'ossigeno di un estere come si deduce
dai valori riportati in tabella B:
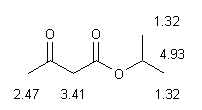
Il segnale successivo è il singoletto di area 2 a 3.41 ppm. E' prodotto da un CH2 che assorbe a frequenze insolitamente alte e questo indica che è compreso tra due carbonili (previsione secondo la Tabella B: 1.0 CO + 1.0 CO + 1.3 CH2 = 3.3 ppm).
Proseguendo verso destra si incontra il
singoletto di area 3 a 2.25 ppm che Indica un CH3
legato al carbonile per il quale la previsione secondo
la tabella B è: 1.0 CO + 1.3 CH2
= 2.3 ppm.
si tratta di 3-oxobutanoato di isopropile.
|
||||||||||||||||
|
|
|||||||||||||||||
|
email: info@pianetachimica.it
|
|||||||||||||||||