|
|
Microtubuli |
|||||
|
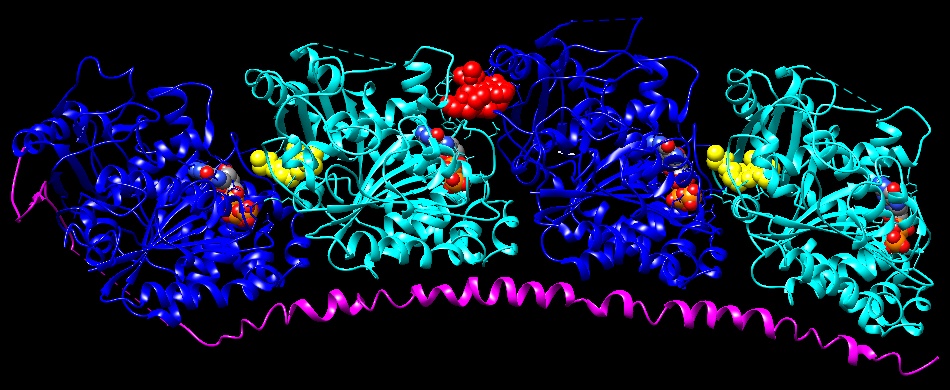
Molecola del Mese di Luglio 2014 I microtubuli sono lunghi filamenti che costituiscono il citoscheletro e sono delle vie di trasporto all'interno della cellula  Introduzione IntroduzioneI microtubuli sono le ferrovie della cellula. Sono costituiti da grossi e robusti filamenti che attraversano il citoplasma e hanno due funzioni: danno stabilità strutturale alla cellula e costituiscono la via lungo la quale si muovono le proteine motrici chinesina e dineina. Le proteine motrici trascinano ogni tipo di carico attraverso la cellula, dalle piccole vescicole ai grandi mitocondri. Hanno anche un ruolo importante nel processo di divisione cellulare separando i cromosomi dopo la duplicazione e trasportandoli ai capi opposti della cellula per generare le due cellule figlie. Tubuli di tubulina I microtubuli sono formati da un gran numero di unità cilindriche della proteina tubulina. La tubulina esiste in due forme simili chiamate tubulina alfa e beta che si legano una all'altra per formare un complesso dimero. Questi poi si impilano uno sull’altro per formare il tubo cilindrico. La struttura del dimero di tubulina (file PDB 1ffx) è mostrata qui sotto con la alfa tubulina a sinistra e la beta tubulina a destra. La struttura mostrata qui a destra, invece, è un mosaico ricostruito al computer (file PDB 3j2u) ottenuto assemblando molte strutture di un dimero di tubulina alfa e beta e usando come modello un'immagine ottenuta con la microscopia elettronica. La struttura mostrata qui a destra rappresenta solo una piccola porzione del filamento vero: nella cellula i microtubuli sono molto più lunghi e sono costituiti da migliaia di subunità di tubulina. . .. 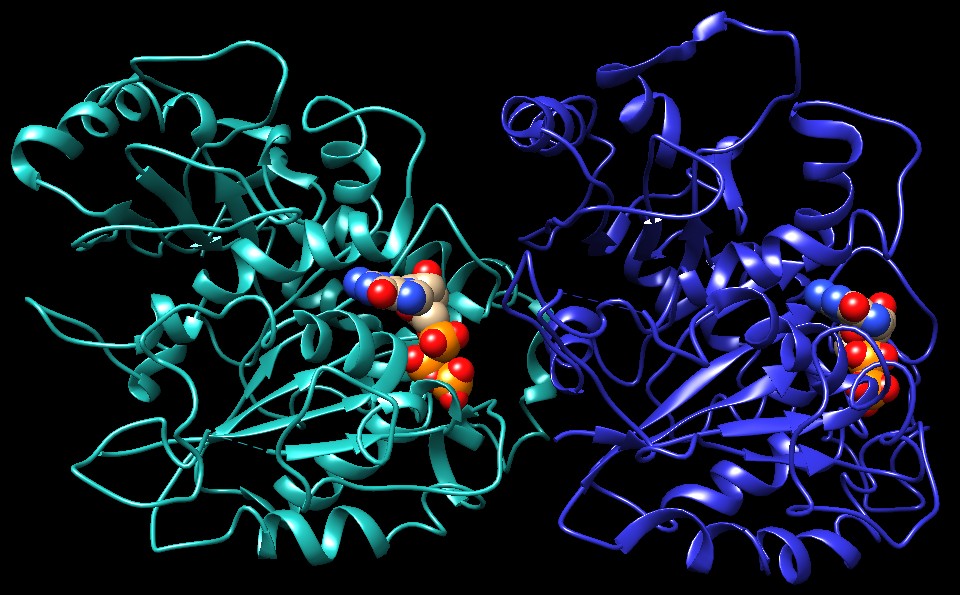 Instabilità dinamica I microtubuli vengono continuamente allungati e accorciati in un processo chiamato di instabilità dinamica. Questo è controllato da una molecola di GTP legata alla tubulina beta. I dimeri di tubulina liberi legano GTP sia sulla catena alfa che sulla beta e, grazie a questo, formano un complesso stabile quando si sommano ad un filamento in crescita. Poco dopo, però, il GTP della catena beta perde un fosfato e si trasforma in GDP. Nella figura qui sopra (file PDB 1ffx) la tubulina alfa (verde sulla sinistra) lega GTP con tre fosfati ben visibili in arancione e rosso. La tubulina beta (blu sulla destra) lega GDP (con due fosfati). La tubulina con GDP sulla catena beta è legata più debolmente al filamento e se si viene a trovare alla fine del microtubulo si stacca e comincia un processo di accorciamento. Se però, nel punto che si sta accorciando, si lega un nuovo dimero di tubulina, il processo si arresta perchè questo possiede GTP sulla catena beta (non ancora degradato a GDP) e il microtubulo ricomincia ad allungarsi.  Aiutare
la tubulina Aiutare
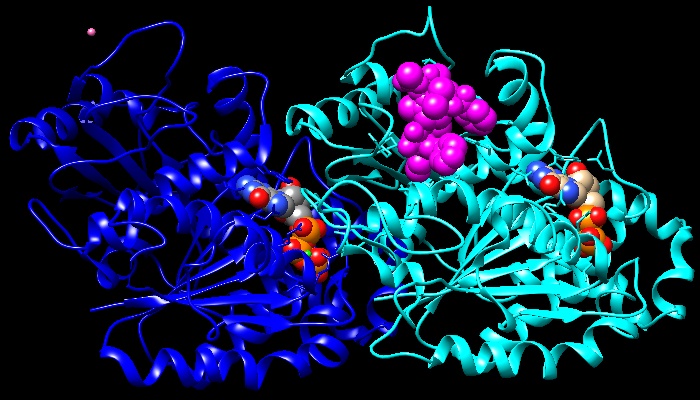
la tubulinaUna grande varietà di proteine aiuta i microtubuli a compiere le loro molte funzioni, vi sono proteine leganti, iniziatrici e regolatrici. La proteina mostrata qui a destra in magenta è la statmina, che destabilizza i microtubuli (file PDB 1ffx). Si lega a due dimeri di tubulina e agisce bloccandoli e impedendo loro di sommarsi, oppure stimolando il loro distacco da un microtubulo che deve accorciarsi. La statmina si è rivelata molto utile per i ricercatori. La tubulina era difficile da studiare con la cristallografia perchè tendeva ad aggregarsi in microtubuli piuttosto che formare cristalli. Il complesso tubulina-statmina, invece, può essere cristallizzato facilmente ed usato per determinare la struttura molecolare della tubulina. 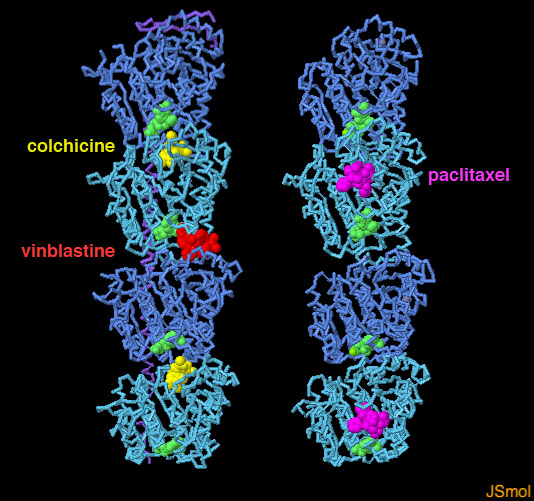 Esplorando
la struttura Esplorando
la strutturaDato che svolgono un ruolo così importante nella divisione cellulare, i microtubuli sono il bersaglio di numerosi veleni e anche di molti farmaci. Alcuni farmaci antitumorali arrestano la rapida crescita delle cellule tumorali bloccando la normale dinamica dei microtubuli. Impediscono che si formi il fuso mitotico e quindi rendono impossibile la duplicazione della cellula. Qui sono mostrate tre molecole, tutte di origine vegetale, che bloccano l'azione dei microtubuli: colchicina (ottenuta dal colchico) e vinblastina (ottenuta dalla pervinca) bloccano la crescita dei microtubuli (file PDB 1z2b); paclitassolo (ottenuto dal tasso) impedisce l'accorciamento dei microtubuli (file PDB 1jff). Nella figura qui sotto (file PDB 1z2b) si vedono due dimeri consecutivi di tubulina alfa-beta (blu-ciano) legati alla proteina statmina (magenta). Vi sono anche la colchicina (gialla) e la vinblastina (rossa) legate tra una catena di tubulina e l'altra. Questa struttura ci rivela come queste due molecole ostacolano la crescita dei microtubuli. La colchicina (gialla) interferisce col legame tra tubulina alfa (blu) e bubulina beta (ciano) all'interno del dimero avvicinandosi molto al GTP della catena alfa. La vinblastina (rossa), invece, si inserisce nel legame tra due dimeri.
Nella prossima figura (file PDB 1jff)
si vede invece il paclitassolo (magenta) che si lega all'interno
della catena di beta tubulina (ciano). Questo sito di legame
suggerisce che il paclitassolo impedisca l'idrolisi del GTP a GDP
rendendo così sempre forte il legame tra i dimeri di tubulina
e impedendo l'accorciamento dei microtubuli che quindi possono solo
crescere. . . . . . . . . .
. . . . . . . . Spunti per ulteriori
esplorazioni
|
||||||
|
|
||||||