|
|
Enzimi mangia-plastica |
|||||
|
Molecola del mese di gennaio 2023 I ricercatori stanno cercando in natura nuovi modi per smaltire i rifiuti di plastica  Introduzione Introduzione
La plastica ha cambiato il nostro mondo perchè ci ha fornito modi nuovi per creare prodotti di largo consumo. La plastica, però, ha anche un grave lato negativo. La maggior parte delle materie plastiche è formata da polimeri stabili chimicamente e quindi quando viene gettata, questi persistono per decenni o per secoli nell'ambiente. L'uso generalizzato della plastica rappresenta una sfida formidabile per l'ambiente e per la salute. I ricercatori, per vincere questa sfida, stanno cercando una via naturale per riciclare e degradare la plastica. Fortunatamente, alcuni batteri sono più avavti di noi e hanno già sviluppato enzimi che possono attaccare alcuni tipi di plastiche. Mangiatori di plastica I due enzimi mostrati qui a lato (file PDB 5xh3 e 6qga) sono stati trovati in un batterio che cresce sulle bottiglie di plastica in discarica. Lavorando insieme, questi due enzimi sono in grado di decomporre il polimero di cui sono fatte le bottiglie, polietilene tereftalato (PET). Questo è un copolimero formato da due diversi monomeri (EG, etilenglicole, e TPA, acido tereftalico) legati tra loro da un legame estere che si alternano nella struttura formando lunghe catene polimeriche. L'enzima PET idrolasi (PETasi) taglia il polimero in pezzi più piccoli (MHET, mono idrossietil tereftalato) che possono essere aggrediti dall'altro enzima, MHET idrolasi (MHETasi), che taglia questi frammenti liberando i singoli monomeri (EG e TPA). Altri enzimi del batterio usano queste semplici molecole come nutrienti per sostenere la crescita del batterio.  Riciclare la plastica Il riciclaggio della plastica non è per niente semplice e pone diversi problemi. I legami che uniscono i monomeri nei vari polimeri (spesso esteri o ammidi) sono stabili chimicamente. Per fortuna molti tipi di enzimi sono in grado di rompere questi legami perchè sono anche i legami che uniscono i biopolimeri come le proteine, gli acidi nucleici e i lipidi. Le plastiche, però, hanno una struttura più densa, con le fibre di polimero impaccate molto strettamente e quindi è difficile per gli enzimi raggiungere quei legami. Una via potrebbe essere quella di scaldare i materiali plastici per ammorbidirli. Per questo i ricercatori stanno cercando di ingegnerizzare gli enzimi naturali per renderli più stabili e capaci di lavorare alle alte temperature. 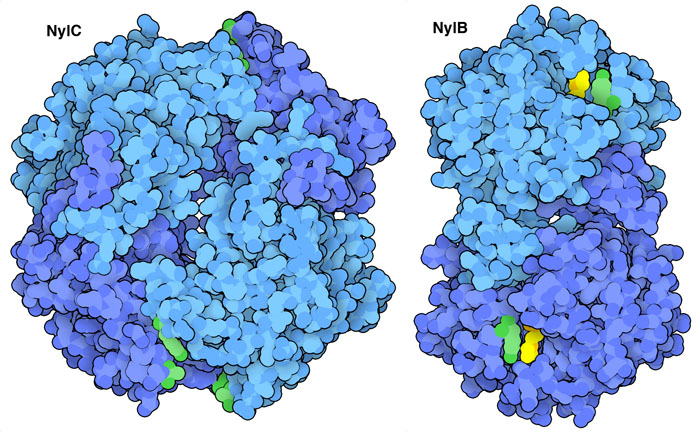 Mangiare
il nylon Mangiare
il nylonLa scoperta dei primi enzimi mangia-plastica ha spinto gli scienziati a cercare altri organismi mangia-plastica. Passando in rassegna molti tipi di batteri, hanno scoperto gli enzimi mostrati qui a fianco che possono tagliare le catene del nylon. Il nylon è costituito da molecole unite da legami ammidici simili a quelli che ci sono tra amminoacidi nelle proteine. Come con gli enzimi PET, la degradazione del nylon si realizza in due passaggi. Un primo enzima NylC taglia il polimero in pezzi più piccoli, un secondo enzima NylB degrada questi frammenti nei loro costituenti elementari. I due enzimi mostrati qui a fianco (file PDB 5y0m e 2zm0) sono stati ingegnerizzati sostituendo alcuni amminoacidi (verdi) per aumentare la loro attività e la stabilità al calore. Esplorando la struttura PET idrolasi ingegnerizzato 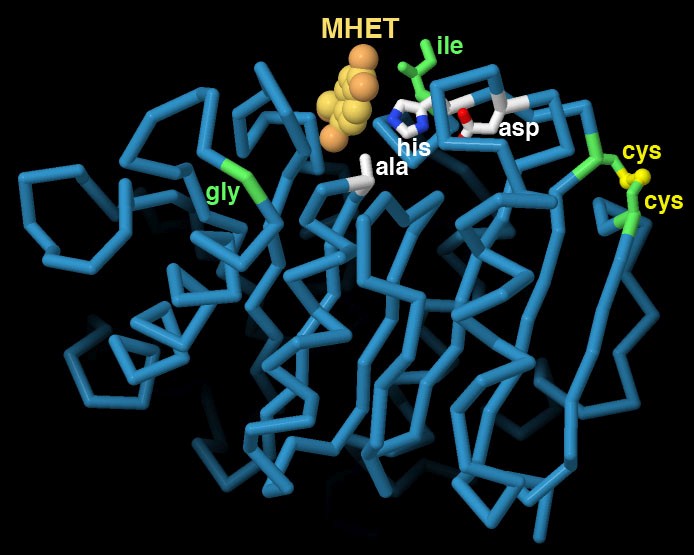 L'enzima
mostrato qui a fianco è un enzima PET idrolasi ingegnerizzato (file
PDB 7vve) che ha una capacità maggiore
di digerire la plastica e una maggiore stabilità termica dell'enzima
nativo. L'enzima
mostrato qui a fianco è un enzima PET idrolasi ingegnerizzato (file
PDB 7vve) che ha una capacità maggiore
di digerire la plastica e una maggiore stabilità termica dell'enzima
nativo. La struttura include una molecola di MHET (acido mono idrossietil tereftalico) legata al sito attivo e mostra come le mutazioni introdotte nell'enzima possono aumentare la sua attività. Due amminoacidi vicini sono stati mutati in cisteina (cys) e così si sono legati tra loro formando un ponte disolfuro che rende l'enzima più stabile al calore. Altre due mutazioni (gly e ile) hanno ridotto le dimensioni di amminoacidi che circondavano il sito attivo e così lo hanno reso più accessibile per le catene del polimero PET. Per tagliare il legame estere l'enzima usa la classica triade di amminoacidi (serina, istidina, acido aspartico: ser, his, asp) che è tipica degli enzimi serina proteasi come la tripsina (mdm 10-2003), l'enzima proteolitico della digestione che produciamo anche noi nel pancreas. Per ottenere questa struttura con l'enzima legato al frammento di polimero intatto, l'enzima è stato disattivato sostituendo la serina del sito attivo con alanina (ala).  Nell'immagine
qui a lato sono mostrate in sequenza le due strutture dell'enzima nativo
(file PDB 4eb0) e di quello ingenerizzato
(file PDB 7vve). Nell'immagine
qui a lato sono mostrate in sequenza le due strutture dell'enzima nativo
(file PDB 4eb0) e di quello ingenerizzato
(file PDB 7vve). Notate che, nel sito attivo, l'enzima nativo ha la serina (che ha un ossigeno rosso) al posto della alanina (ala, bianca). Inoltre ha due amminoacidi aromatici ingombranti (verdi). Sulla destra, l'enzima nativo ha due amminoacidi (verdi) che non sono legati tra loro. . . . . . . . . . . . . . . . . . . . Spunti per ulteriori esplorazioni Negli archivi PDB si trovano molte strutture di enzimi mangia plastica ingegnerizzati. Per trovarle, cominciate cercando uno qualsiasi di questi enzimi e poi usate l'opzione "Find similar proteins by: Sequence" nella sezione "Macromolecules". Le mutazioni coinvolgono pochi amminoacidi e quindi una somiglianza dell' 80% o del 90% tra le sequenze vi consente di trovare la lista degli enzimi mutati. Potete confrontare le strutture mutate con quelle native usando l'opzione "Pairwise Structure Alignment" nel menù "Analyze" Chow, J., Perez-Garcia, P., Dierkes, R., Streit, W.R. (2022) Microbial enzymes will offer limited solutions to the global plastic pollution crisis. Microbial Biotechnology doi: 10.1111/1751-7915.14135 7vve: Zeng, W., Li, X., Yang, Y., Min, J., Huang, J.-W., Liu, W., Niu, D., Yang, X., Han, X., Zhang, L., Dai, L., Chen, C.-C., Guo, R.-T. (2022) Substrate-Binding Mode of a Thermophilic PET Hydrolase and Engineering the Enzyme to Enhance the Hydrolytic Efficacy. ACS Catal 12: 3033-3040 6qga: Palm, G.J., Reisky, L., Bottcher, D., Muller, H., Michels, E.A.P., Walczak, M.C., Berndt, L., Weiss, M.S., Bornscheuer, U.T., Weber, G. (2019) Structure of the plastic-degrading Ideonella sakaiensis MHETase bound to a substrate. Nat Commun 10: 1717 5y0m: Negoro, S., Shibata, N., Lee, Y.H., Takehara, I., Kinugasa, R., Nagai, K., Tanaka, Y., Kato, D.I., Takeo, M., Goto, Y., Higuchi, Y. (2018) Structural basis of the correct subunit assembly, aggregation, and intracellular degradation of nylon hydrolase. Sci Rep 8: 9725-9725 5xh3: Han, X., Liu, W., Huang, J.W., Ma, J., Zheng, Y., Ko, T.P., Xu, L., Cheng, Y.S., Chen, C.C., Guo, R.T. (2017) Structural insight into catalytic mechanism of PET hydrolase. Nat Commun 8: 2106-2106 2zm0: Kawashima, Y., Ohki, T., Shibata, N., Higuchi, Y., Wakitani, Y., Matsuura, Y., Nakata, Y., Takeo, M., Kato, D., Negoro, S. (2009) Molecular design of a nylon-6 byproduct-degrading enzyme from a carboxylesterase with a beta-lactamase fold. FEBS J 276: 2547-2556
|
||||||
|
|
||||||
