|
|
Catalasi |
|||||
|
Molecola del mese di settembre 2004 La catalasi ci protegge dall'acqua ossigenata, una molecola ossidante pericolosa e reattiva, che trasforma in acqua e O2  Introduzione IntroduzioneVivere con l'ossigeno è pericoloso. Noi lo utilizziamo per produrre energia nelle nostre cellule, ma l'ossigeno è una molecola molto reattiva che può provocare problemi seri se non viene tenuta strettamente sotto controllo. Uno dei pericoli maggiori nasce dal fatto che l'ossigeno può essere convertito facilmente in altri composti molto reattivi. Nelle nostre cellule gli elettroni vengono continuamente trasportati da un luogo all'altro da molecole trasportatrici di elettroni, come i citocromi, il coenzima Q o il FAD e il NAD che contengono rispettivamente riboflavina e niacina (vitamina B2 e B3). Se l'ossigeno incontra uno di questi trasportatori, può catturare accidentalmente un elettrone. Questo converte l'ossigeno in composti pericolosi come i radicali superossido e l'acqua ossigenata che attaccano e ossidano i delicati atomi di zolfo e gli ioni dei metalli nelle proteine. A peggiorare la situazione, gli ioni ferro liberi nella cellula talvolta convertono l'acqua ossigenata in radicali idrossido. Questi sono ancora più pericolosi e attaccano e mutano il DNA. Una teoria, ancora controversa, dice che questo tipo di danno ossidativo si accumula negli anni durante la nostra vita, causando l'invecchiamento. Antiossidanti indispensabili Velocissima e stabile
 Esplorando
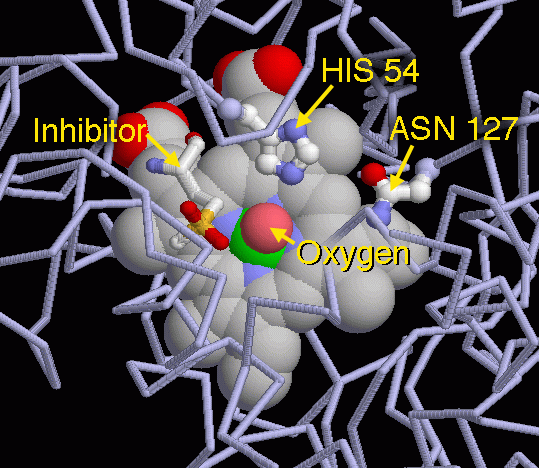
la struttura Esplorando
la struttura La catalasi compie la sua rapida azione di distruzione dell'acqua ossigenata in due tappe successive. Nella prima tappa, l'enzima lega una molecola di acqua ossigenata e la spezza in due frammenti diversi. Il primo è un atomo di ossigeno che rimane legato al ferro dell'eme, ed il secondo frammento viene rilasciato come semplice acqua. Nella seconda tappa, l'enzima lega un'altra molecola di acqua ossigenata. Anche questa viene spezzata in due frammenti diversi. L'ossigeno viene combinato con l'altro atomo di ossigeno già legato al ferro producendo ossigeno gassoso O2.. La parte restante viene rilasciata come acqua. Nella figura qui a fianco (file PDB 2cag) è rappresentata la catalasi nel mezzo di questa reazione a due tappe. Il primo atomo di ossigeno è già legato al ferro, pronto per legarsi alla seconda molecola di acqua ossigenata. Gli amminoacidi istidina 54 e asparagina 127 aiutano la reazione. La piccola molecola sulla sinistra è un inibitore che i ricercatori hanno usato per bloccare l'enzima in questa forma significativa, dando così loro il tempo necessario per studiarla.
|
||||||
|
|
||||||

 Catalasi
diverse
Catalasi
diverse