|
|
DNA elicasi |
|||||
|
Molecola del Mese di Dicembre 2013 La DNA elicasi separa i due filamenti del DNA a doppia elica e scorre lungo uno dei due filamenti spinta da ATP  Introduzione IntroduzioneLe informazioni genetiche sono custodite nella doppia elica del DNA. Per utilizzare queste informazioni, però, l'elica deve essere aperta per esporre le basi azotate, consentendo l'accesso alla DNA polimerasi (mdm 3/2000) e alla RNA polimerasi per costruire nuove catene di DNA o di RNA complementari. Separare i due filamenti di DNA è più complicato di quanto possa sembrare, perchè i filamenti di DNA sono formati da sequenze lunghissime di basi azotate. Inoltre ogni base è legata alla propria complementare da legami idrogeno relativamente forti e quindi serve molta energia per separare i due filamenti. Questo compito è svolto della DNA elicasi, un enzima specializzato nel separare i due filamenti della doppia elica del DNA. Elicasi di replicazione La elicasi batterica mostrata qui a destra (file PDB 4esv) separa i due filamenti del DNA durante la replicazione del genoma. Il cromosoma dei batteri è circolare e la replicazione comincia in un punto dell'anello chiamato ORI (origine di replicazione) e procede in entrambe le direzioni per finire sul lato opposto. L'elicasi circonda una porzione a singolo filamento del DNA (mostrata qui in marroncino) e avanza lungo il DNA spendendo ATP (rosso) e separando i due filamenti davanti a sè. In questo modo fa avanzare la separazione tra i due filamenti che viene chiamata forcella di replicazione. Circondare il DNA La DNA elicasi di replicazione appartiene ad una grande classe di proteine che usano ATP per far avanzare un anello proteico lungo un filamento di acidi nucleici o di proteine. Questi enzimi si dividono in due categorie: quelli batterici sono simili a RecA, una proteina coinvolta nella ricombinazione genetica, mentre le nostre elicasi di replicazione sono AAA+ ATPasi, come quelle contenute nelle AAA+ proteasi (mdm 8-2006). In tutti e due i casi il complesso forma un anello di subunità che circonda il singolo filamento di DNA. L'elicasi di replicazione mostrata qui sopra è formata di sei subunità identiche che formano un complesso a forma di ciambella che circonda l'elica a singolo filamento del DNA lungo il quale è capace di muoversi spendendo ATP. L'avanzamento avviene passo-passo con la rottura sequenziale di ATP nelle diverse subunità che provoca un avanzamento sequenziale di una subunità alla volta per due nucleotidi nella direzione 5'-3'.  Sciogliere
il DNA Sciogliere
il DNADue proteine aiutano l'elicasi di replicazione ad iniziare il suo lavoro. La prima, conosciuta come iniziatore, si lega all'origine di replicazione e fa legare l'elicasi nella giusta posizione. DnaA è la proteina iniziatore mostrata qui (file PDB 3r8f) e realizza anche la separazione iniziale delle due catene. E' formata da una lunga elica di subunità e si pensa che svolga due compiti diversi. Inizialmente riconosce una speciale sequenza nell'origine ORI che è ricca di paia di basi AT (che sono legate tra loro più debolmente delle coppie GC) e si lega in questo punto avvolgendosi all'esterno della doppia elica del DNA, formando una struttura a superelica. Poi DnaA separa le due catene ricche di paia di basi AT, catturando e stirando uno dei due filamenti come si vede nella struttura qui a lato. 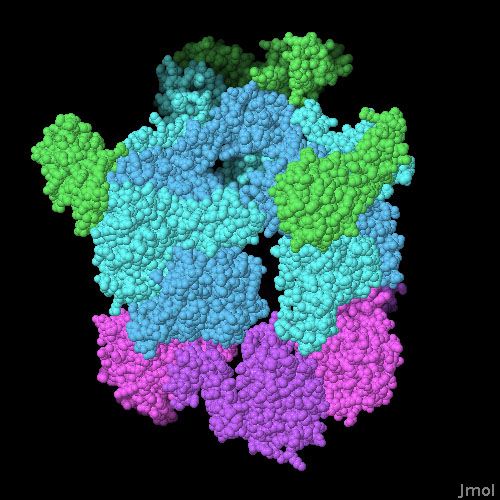 Esplorando la struttura
Esplorando la strutturaUna ulteriore proteina aiuta la DNA elicasi di replicazione a legarsi al singolo filamento di DNA: il caricatore di elicasi (mostrato qui a fianco in basso in magenta). La struttura mostrata qui a destra (file PDB 4m4w) è davvero complessa e include molte subunità: la DNA elicasi (blu e azzurra), il caricatore di elicasi (magenta) un piccolo frammento di primasi (verde). La primasi è l'enzima che costruisce il breve tratto di RNA chiamato primer che consente alla DNA polimerasi di iniziare la duplicazione. Tutte queste proteine costituiscono una struttura troppo complessa per essere determinata ad alta risoluzione con la tecnica della diffrazione ai raggi X. La struttura qui a lato è stata ottenuta assemblando al computer molte strutture ottenute separatamente. I singoli componenti ad alta risoluzione sono stati uniti tra loro utilizzando un modello a bassa risoluzione ottenuto al microscopio elettronico. Si noti il foro al centro dell'anello delle subunità della elicasi dove passa il singolo filamento di DNA. Potete vedere in azione il complesso enzimatico elicasi-primasi-DNA polimerasi nella seguente animazione dove si vede la duplicazione del DNA con la produzione di una catena veloce e di una catena lenta fatta unendo i frammenti di Okazaki. Duplicazione del DNA (animazione di cui nella figura qui sotto è mostrato un fotogramma) www.wehi.edu.au/wehi-tv/molecular-visualisations-dna . . . . . . . . . . . . . . . . . . . .  Spunti per ulteriori esplorazioni Negli archivi PDB si possono trovare molte altre strutture di elicasi legate ad un tratto di DNA a singolo filamento, compresa la DNA elicasi batterica Rep che agisce come dimero (file PDB 1uaa). DnaA ha un dominio che si lega al DNA a doppia elica, inserendosi con un tratto ad alfa elica nella scanalatura maggiore e con un altro tratto in quella minore, in corrispondenza di una particolare sequenza di basi AT in ORI e in questo modo dà inizio alle operazioni di replicazione. Una struttura che illustra questo legame è PDB 1j1v. La struttura dal caricatore di elicasi DnaC è molto simile a quella di DnaA, infatti forma una serie quasi uguale di subunità ad alfa elica. Usate lo strumento "Compare Structures" per sovrapporre queste due strutture PDB: 3ecc e 3r8f. 4m4w: B. Liu, W. K. Eliason & T. A. Steitz (2013) Structure of a helicase-helicase loader complex reveals insights into the mechanism of bacterial primosome assembly. Nature Communications 4: 2495. 4esv: O. Itsathitphaisarn, R. A. Wing, W. K. Eliason, J. Wang & T. Steitz (2012) The hexameric helicase DnaB adopts a nonplanar conformation during translocation. Cell 151, 267-277. P. Soultanas (2012) Loading mechanisms of ring helicases at replication origins. Molecular Microbiology 84, 6-16. 3r8f: K. E. Duderstadt, K. Chuang & J. M. Berger (2011) DNA stretching by bacterial initiators promotes replication origin opening. Nature 478, 209-213.
|
||||||
|
|
||||||
