|
|
AAA+ Proteasi |
|||||
|
Molecola del Mese di Agosto 2006 Le AAA+ proteasi sono macchine molecolari spinte da ATP che trasportano le proteine da degradare attraverso un foro e poi le idrolizzano  AAA+
Proteasi AAA+
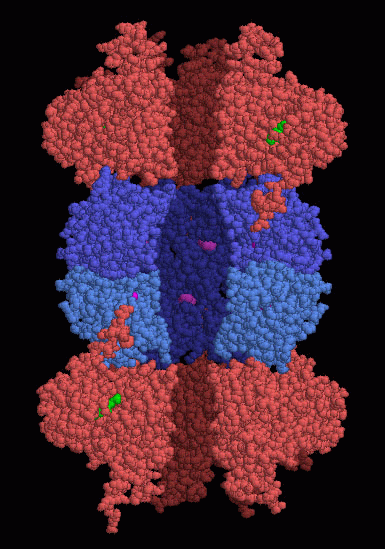
ProteasiCome si può costruire un enzima in grado di tagliare le proteine, ma che sia anche sicuro da usare all'interno delle cellule? Le proteasi della digestione come la tripsina (mdm 10-2003) e la pepsina (mdm 12-2000) sono enzimi piccoli ed efficienti che diffondono liberamente all'interno del cibo che stiamo digerendo fino a raggiungere le proteine e quindi le tagliano in pezzi. Enzimi di questo tipo sarebbero distruttivi se agissero in modo incontrollato all'interno della cellula. La cellula deve avere il massimo controllo sulla degradazione delle proteine in modo che solo le proteine inutili o danneggiate vengano distrutte. Le proteasi AAA+ risolvono questo problema in modo elegante. Utilizzano una doppia strategia per assicurarsi che solo certe proteine vengano distrutte. Per prima cosa, gli enzimi che tagliano le proteine sono nascosti all'interno di un contenitore chiuso e, secondo, usano una speciale pompa proteica per far entrare le proteine nella camera di distruzione. Il loro nome deriva proprio da questa pompa chiamata AAA+, cioè ATPasi Associata con Attività cellulari. Shock Termico Attualmente, le strutture più complete di AAA+ proteasi sono state ottenute dalla proteina batterica HSLUV (da Heat Shock Locus prodotti genetici U e V) mostrata qui a destra (file PDB 1yyf). Questa è composta da due tipi di subunità proteiche. Le subunità di proteasi formano lo stretto cilindro centrale (blu). I loro siti attivi che tagliano le proteine sono tutti rivolti verso la parte interna del cilindro. Le subunità AAA+ ATPasi (rosse e arancioni) controllano l'ingresso ai due lati del cilindro centrale. La proteina HSLUV è una delle molte proteine da shock termico che vengono sintetizzate quando la cellula subisce un riscaldamento a livelli pericolosi. Il calore eccessivo fa srotolare le proteine che possono poi ripiegarsi in modo errato o aggregarsi tra loro. Per questo motivo, in caso di shock termico, vengono sintetizzati un gran numero sia di chaperon (mdm 8-2002) che di proteasi. I Chaperon servono per aiutare le proteine a ripiegarsi in modo corretto. Le Proteasi per distruggere le proteine danneggiate dal calore. Proteasoma Le nostre cellule costruiscono una versione più complessa della HSLUV: il proteasoma. Questo ha al centro una camera di distruzione più grande della HSLUV composta da un gruppo di quattro complessi proteici a forma di anello. Ad ogni lato c'è un meccanismo che cerca le proteine marcate con l'ubiquitina e poi utilizza molecole simili alla AAA+ ATPasi per condurre le proteine nella camera centrale. Per ulteriori informazioni su questo meccanismo, potete vedere la molecola del mese ubiquitina (12-2004). 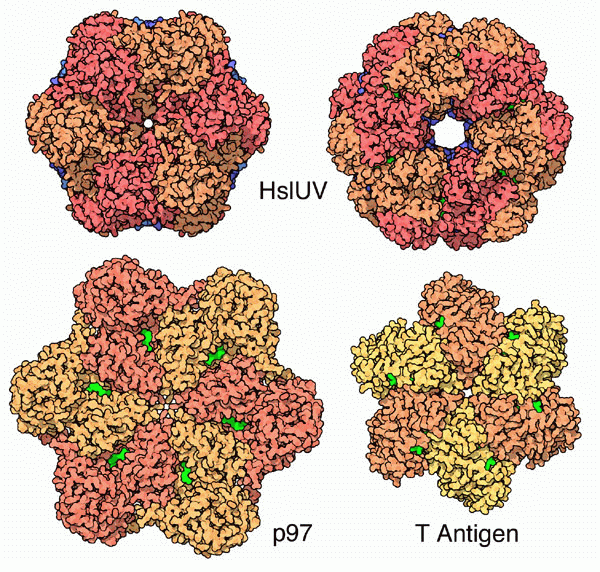 AAA+
ATPasi AAA+
ATPasiLa pompa per le proteine della HSLUV è costituita da un anello di sei subunità che circondano un canale centrale. Come si può vedere nelle due strutture mostrate qui a destra in alto (file PDB 1yyf e 1g3i), questi anelli possono cambiare di molto le loro dimensioni e per questo utilizzano ATP. Una proteasi simile, CLPXP, utilizza da 30 a 80 molecole di ATP (a seconda di quanto stabile è la proteina) per spingere una catena di 100 amminoacidi attraverso il suo canale centrale. Le ATPasi ad anello, chiamate AAA+, sono molto comuni nelle cellule dove vengono usate per svolgere una serie di compiti simili. Negli archivi PDB sono disponibili molte ATPasi di questo tipo: l'antigene T del virus Simian 40 (file PDB 1svm) che svolge la doppia elica del DNA, il p97 (file PBD 1oz4 o 1r7r) e il NSF (file PDB 1nsf o 1d2n) che degradano i complessi proteici coinvolti nel trasporto di membrana. La dineina (mdm 8-2014), un noto motore proteico, e la DNA elicasi (mdm 12-2013) un enzima specializzato nel separare i due filamenti della doppia elica del DNA, hanno una struttura simile alla AAA+ ATPasi per generare il loro movimento.
|
||||||
|
|
||||||

 Esplorando
la Struttura
Esplorando
la Struttura