|
|
Vitamine |
|||||
|
Molecola del mese di dicembre 2023 Le vitamine sono degli strumenti molecolari indispensabili che possiamo ottenere solo con la dieta. 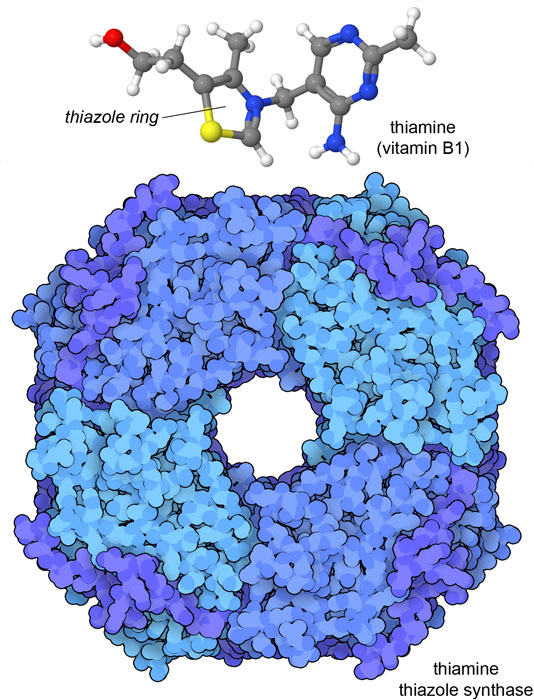 Introduzione IntroduzioneUna dieta sana deve comprendere tutti i nutrienti di cui abbiamo bisogno per far crescere le nostre cellule in salute. Questi includono proteine, carboidrati, acidi nucleici e grassi che, prima, vengono tagliati in frammenti più semplici e poi vengono usati sia per costruire le molecole del nostro corpo, sia per fornirci l'energia di cui abbiamo bisogno per vivere. Con la dieta dobbiamo assumere anche molti minerali come il ferro per sintetizzare l'emoglobina (mdm 5-2003) o il calcio per costruire le ossa (mdm 4-2029). Inoltre, dobbiamo assumere piccole quantità di 13 vitamine essenziali. Le vitamine sono molecole piccole e dalla struttura particolare che servono ad assolvere compiti speciali nelle nostre cellule. Queste molecole sono necessarie per la vita, ma le nostre cellule non sono in grado di produrle e, quindi, dobbiamo assumerle con la dieta. Evoluzione delle vitamine Se le vitamine sono così importanti, perchè il nostro corpo non è in grado di produrle? La risposta si trova nello studio dell'evoluzione. I nostri antichi antenati potevano trovare queste molecole molto facilmente nei cibi della loro dieta, quindi non c'era una forte necessità di produrli da zero. Inoltre, molte di queste molecole sono complicate da sintetizzare, così c'è stata una spinta selettiva per evitare di sprecare risorse per produrle. Quindi, nei nostri antichi antenati evolutivi, la sicurezza di avere queste molecole disponibili non è stata sufficiente a compensare i costi della loro sintesi e così la capacità di sintetizzarle è stata persa per sempre. Enzimi suicidi L'enzima che sintetizza la vitamina B1 (tiamina) è un buon esempio di questa tendenza evolutiva. Nelle piante e nelle cellule del lievito, lo strano anello tiazolico è prodotto dall'enzima tiamina-tiazolo-sintasi. Quando i ricercatori hanno studiato la struttura di questo enzima (mostrato qui a lato dal file PDB 3fpz), hanno scoperto che un amminoacido di cisteina, cys 205, era privo del suo atomo di zolfo. Ulteriori studi hanno rivelato che questo enzima aveva donato lo zolfo per la sintesi dell'anello tiazolico. Questo significa che l'enzima tiamina-tiazolo-sintasi è un enzima suicida che può operare una volta soltanto. Per questa ragione, sintetizzare la tiamina è molto costoso e le cellule di lievito devono produrre grandi quantità di questa proteina. Poichè noi ( e altri animali) mangiamo piante che hanno molta tiamina, non dobbiamo per forza sopportare il costo di sintetizzare questo enzima usa e getta per produrre una nostra tiamina.  Conseguenze mortali Le vitamine sono state scoperte studiando le malattie storiche che colpivano le persone che avevano una dieta priva di queste molecole. Per esempio, i marinai. che nei secoli scorsi compivano lunghi viaggi in mare, si ammalavano di scorbuto, una malattia provocata dall'incapacità di produrre il collagene (mdm 4-200). La causa era la mancanza di vitamina C (acido ascorbico) nella loro dieta e il problema alla fine è stato risolto imbarcando una grande quantità di agrumi per il viaggio. Oggi abbiamo capito i dettagli molecolari di questa malattia. L'enzima collagene-prolil-4-idrossilasi (mostrato qui a lato dai file PDB 7zsc e 4bta) converte la prolina della catena di collagene in idrossiprolina che è essenziale per impaccare strettamente le catene di collagene e per farle aderire una all'altra nel tessuto connettivo sano. L'enzima usa un complesso ferro-zolfo (mdm 5-2007) per questa reazione, ma talvolta una reazione collaterale indesiderata ossida il ferro (da 2+ a 3+) e inattiva il complesso. E' qui che entra in gioco la vitamina C che è un potente antiossidante e ripristina il corretto stato di ossidazione degli atomo di ferro (da 3+ a 2+) e così riattiva l'enzima. 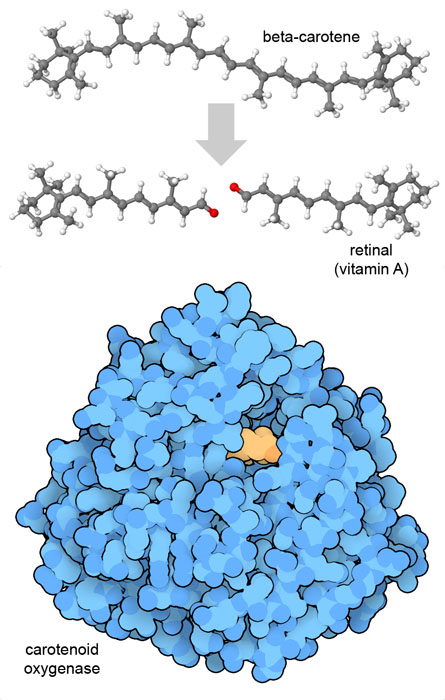
Mangiate carote! Noi otteniamo la maggior parte delle vitamine dai cibi della nostra dieta, inoltre oggi molti cibi processati sono arricchiti con vitamine per aiutarci ad assumerne la corretta dose giornaliera. In molti casi otteniamo queste vitamine direttamente dal cibo perchè anche le piante e gli animali che mangiamo usano le vitamine per realizzare le reazioni nelle loro cellule. In alcuni casi siamo in grado di sintetizzare una vitamina a partire da una molecola che serviva per uno scopo diverso. Per esempio, nelle piante ci sono molecole come il beta-carotene che hanno un colore brillante perchè devono assorbire alcune lunghezze d'onda della luce. Le carote sono una delle sorgenti più note di beta-carotene, la molecola responsabile del loro colore arancione. Le nostre cellule usano l'enzima carotene-ossigenasi per tagliare il carotene in due pezzi uguali di vitamina A (retinale). Anche il retinale assorbe la luce ed è usato nei nostri occhi per la sintesi della rodopsina (mdm 3-2012), la proteina recettore della luce nella retina. Qui a lato è mostrato un enzima dei cianobatteri che ha una struttura simile a quello umano che sintetizza il retinale (file PDB 2biw) 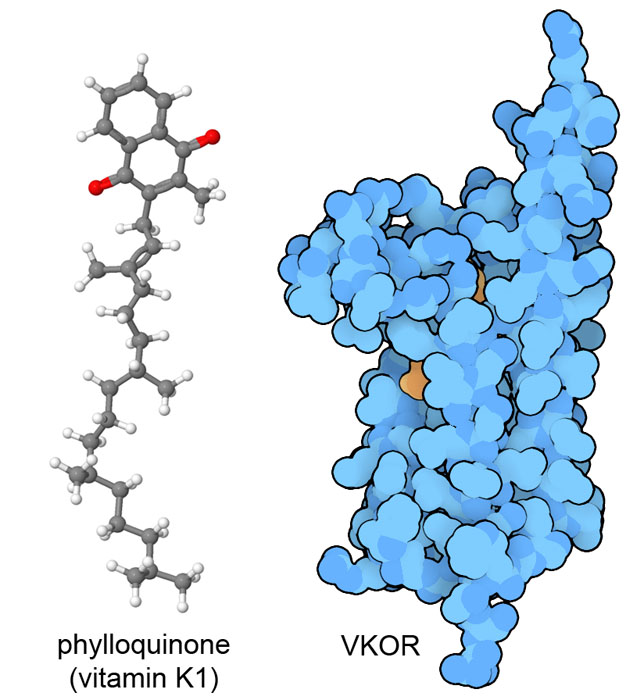
Segreti del mestiere Ogni vitamina ha caratteristiche diverse. La vitamina A è una specialista: è la molecola sensibile alla luce nei nostri occhi. Le vitamine B sono generaliste: fanno entrare od uscire gruppi chimici (o elettroni) dalle molecole e sono usate da molti enzimi diversi. Le vitamine C ed E sono antiossidanti e proteggono le molecole. La vitamina D è un ormone che trasporta messaggi. La vitamina K è utilizzata da enzimi che modificano l'amminoacido glutammato in proteine coinvolte nella coagulazione del sangue, come il Fattore X (mdm 3-2006), e le rende capaci di aderire alla superficie delle cellule. Qui a fianco è mostrata la vitamina K1 e l'enzima VKOR (vitamina K epossido reduttasi dal file PDB 6wv5) che catalizza questa reazione e che è il bersaglio di un potente anticoagulante, warfarina. La vitamina K può assumere diverse forme, quella chiamata fillochinone ha una funzione molto diversa nelle piante dove fa da trasportatore di elettroni nel fotosistema I. 
Costruire gli strumenti Le vitamine B sono una famiglia di vitamine usate per portare dentro o fuori dalle molecole gruppi chimici o elettroni e quindi devono essere posizionate con precisione dagli enzimi che le usano. Dato però che molte vitamine B sono piccole e difficili da maneggiare, le cellule le uniscono ad opportune maniglie chimiche. Per esempio, la riboflavina (vitamina B2) viene legata ad un nucleotide per formare il FAD (flavin adenin dinucleotide). La niacina (vitamina B3) viene unita ad un nucleotide simile per formare il NADH. Qui a fianco sono mostrati i due enzimi che trasformano la riboflavina in FAD: il primo, riboflavina-chinasi (file PDB 1p4m), aggiunge un fosfato, il secondo, FAD-sintetasi (file PDB 2wsi), aggiunge il nucleotide. 
Vitamine autoprodotte Due vitamine (B3 e D) hanno un posto di rilievo in questa lista. Le nostre cellule sono in grado di sintetizzarle, ma non in quantità sufficiente. La niacina (vitamina B3) serve per sintetizzare il principale trasportatore di elettroni, il NADH, che è usato in quasi tutti i processi di biosintesi e di produzione di energia. Il NADH trasporta elettroni provenienti dalla glicolisi (mdm 2-2004) e dal ciclo dell'acido citrico (Krebs) (mdm 10-2012) verso la NADH-deidrogenasi del Complesso 1 (mdm 12-2011) della catena respiratoria. Le nostre cellule possono sintetizzare la niacina a partire dall'amminoacido triptofano, ma il processo è poco efficiente e quindi la maggior parte della niacina la otteniamo con la dieta. La vitamina D è prodotta nella pelle quando una forma di colesterolo viene trasformato chimicamente per esposizione ai raggi UV del sole. Questo processo è sufficiente se viviamo in un posto soleggiato, altrimenti abbiamo bisogno di una fonte diretta di vitamina D come l'olio di fegato di merluzzo. 
Trasporti speciali In alcuni casi il nostro corpo deve usare strategie speciali per far arrivare la vitamina nei distretti del corpo dove serve. Per esempio, la vitamina E (tocoferolo) è un antiossidante solubile nei grassi che protegge le membrane cellulari dall'ossidazione da parte dei perossidi. Dato che non è solubile in acqua, dobbiamo sintetizzare una proteina per trasportare il tocoferolo attraverso il flusso sanguigno fino ai i tessuti che ne hanno bisogno. Nella figura qui a lato è mostrata una di queste proteine (tocoferolo transfer protein, file PDB 3w67) che ingloba la vitamina E (viola) al suo interno e un fosfolipide (verde) che aiuta la proteina a rilasciare la vitamina quando è giunta a destinazione. Esplorando la struttura: vitamina B12 in azione La vitamina B12 (cobalammina) è la più grande tra le vitamine ed è usata da un ristretto numero di enzimi nelle nostre cellule. L'enzima, di cui qui sotto sono mostrati due particolari, è il metilmalonil-coenzima-A-mutasi (file PDB 4req) che trasforma l'acido 2-metilmalonico in acido succinico rimuovendo il metile (giallo) che sporge dal C-2 dell'acido metilmalonico e lo ingloba nella catena di carboni ottenendo così acido succinico che ha la catena di carboni (gialla) più lunga di una unità. Durante la reazione, la molecola è tenuta vicina alla vitamina B12 legandola come tioestere al coenzima A che, a sua volta, è costruito usando la vitamina B5 (acido pantotenico). Questo è un passaggio importante nella degradazione degli amminoacidi che vengono convertiti ad acido succinico che poi è degradato nel ciclo dell'acido citrico (Krebs) (mdm 10-2012). Questa struttura include entrambi gli stati della molecola. La reazione è catalizzata dall'atomo di cobalto che si trova al centro della vitamina B12, con l'aiuto di una molecola vicina di deossiadenosina. 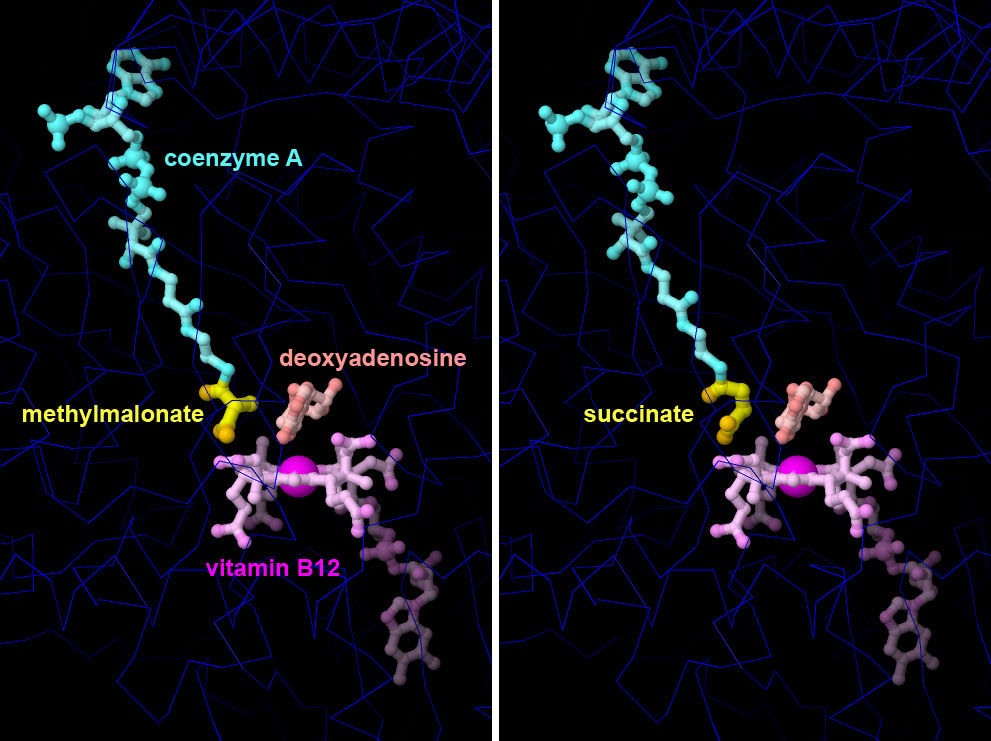 Spunti per ulteriori esplorazioni Negli archivi PDB sono presenti molte strutture che includono vitamine. Potete trovarle cercando una vitamina, andando nella pagina dei legandi, e usando l'opzione "is present as a standalone ligand.". Qui, per esempio, c'è la pagina della vitamina B12 che si trova in oltre cento file PDB. Per trovare più informazioni sulle fonti e sui benefici per la salute delle vitamine, cercate alla pagina: US National Library of Medicine. 7zsc: Murthy, A.V., Sulu, R., Lebedev, A., Salo, A.M., Korhonen, K., Venkatesan, R., Tu, H., Bergmann, U., Janis, J., Laitaoja, M., Ruddock, L.W., Myllyharju, J., Koski, M.K., Wierenga, R.K. (2022) Crystal structure of the collagen prolyl 4-hydroxylase (C-P4H) catalytic domain complexed with PDI: Toward a model of the C-P4H alpha 2 beta 2 tetramer. J Biol Chem 298: 102614-102614 6wv5: Liu, S., Li, S., Shen, G., Sukumar, N., Krezel, A.M., Li, W. (2021) Structural basis of antagonizing the vitamin K catalytic cycle for anticoagulation. Science 371: eabc5667 4bta: Anantharajan, J., Koski, M.K., Kursula, P., Hieta, R., Bergmann, U., Myllyharju, J., Wierenga, R.K. (2013) The structural motifs for substrate binding and dimerization of the alpha subunit of collagen prolyl 4-hydroxylase. Structure 21: 2107-2118 Helliwell, K.E., Wheeler, G.L., Smith, A.G. (2013) Widespread decay of vitamin-related pathways: coincidence or consequence? Trends Genetics 29, 469-478. 3w67: Kono, N., Ohto, U., Hiramatsu, T., Urabe, M., Uchida, Y., Satow, Y., Arai, H. (2013) Impaired alpha-TTP-PIPs interaction underlies familial vitamin E deficiency. Science 340: 1106-1110 3fpz: Chatterjee, A., Abeydeera, N.D., Bale, S., Pai, P.J., Dorrestein, P.C., Russell, D.H., Ealick, S.E., Begley, T.P. (2011) Saccharomyces cerevisiae THI4p is a suicide thiamine thiazole synthase. Nature 478: 542-546 2wsi: Leulliot, N., Blondeau, K., Keller, J., Ulryck, N., Quevillon-Cheruel, S., Van Tilbeurgh, H. (2010) Crystal structure of yeast FAD synthetase (Fad1) in Complex with Fad. J Mol Biol 398: 641-646 2biw:Kloer, D.P., Ruch, S., Al-Babili, S., Beyer, P., Schulz, G.E. (2005) The structure of a retinal-forming carotenoid oxygenase. Science 308: 267-269 1p4m: Karthikeyan, S., Zhou, Q., Mseeh, F., Grishin, N.V., Osterman, A.L., Zhang, H. (2003) Crystal structure of human riboflavin kinase reveals a beta barrel fold and a novel active site arch. Structure 11: 265-273 4req: Mancia, F., Evans, P.R. (1998) Conformational changes on substrate binding to methylmalonyl CoA mutase and new insights into the free radical mechanism. Structure 6: 711-720
|
||||||
|
|
||||||
