|
Molecola del mese
di marzo 2025
Enzimi che possono fissare il carbonio
in modo rapido ed efficiente
 Introduzione Introduzione
La fissazione del carbonio è un processo biologico cruciale che
trasforma l'anidride carbonica (CO2), una molecola abbondante ma biologicamente
inaccessibile, in composti organici come gli zuccheri. La maggior parte
della fissazione del carbonio è realizzata da piante e alghe
attraverso l'enzima Rubisco. La Rubisco, tuttavia, è un enzima
relativamente lento e inefficiente (mdm 9-2000 e 9-2024).
Questa inefficienza ha guidato adattamenti evolutivi in alghe e piante,
come la produzione di grandi quantità di Rubisco e il suo stoccaggio
in organelli specializzati (ad esempio, pirenoidi e cloroplasti). L'inefficienza
della Rubisco è, in gran parte, dovuta all'affinità sia
per la CO2 sia per l'ossigeno molecolare O2, entrambi presenti ad alte
concentrazioni nell'atmosfera terrestre. Nonostante vari tentativi di
laboratorio per migliorare l'efficienza della Rubisco, miglioramenti
significativi rimangono elusivi. La fissazione del carbonio, tuttavia,
non è esclusiva di piante e alghe. Alcuni batteri e archaea hanno
sviluppato vie alternative di fissazione del carbonio che non si basano
sulla Rubisco. Lo studio di questi sistemi può fornire informazioni
su come potremmo progettare sistemi sintetici per catturare e fissare
l'anidride carbonica dalla nostra atmosfera, un passo importante verso
la riduzione della CO2 atmosferica.
Un modo più efficiente per fissare
il carbonio
Una famiglia di enzimi scoperta relativamente di recente, nota come
enoil-CoA carbossilasi/reduttasi (ECR), che può essere
trovata in alcune specie di batteri e archaea, è in grado di
catalizzare la fissazione del carbonio a velocità eccezionalmente
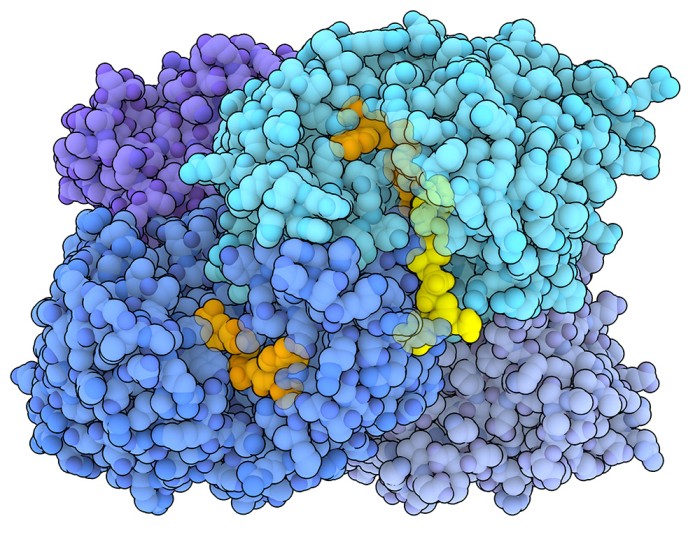
elevate. Una ECR di un batterio del suolo chiamato Kitasatospora setae
(PDB 6OWE) è mostrata qui sopra.
A differenza della Rubisco, le ECR non accettano O2 come substrato,
evitando così la possibile competizione con la CO2. Sorprendentemente,
si è scoperto che le ECR superano la Rubisco fino a 10 volte
in termini di velocità di reazione. Recenti studi strutturali
hanno dimostrato che le ECR funzionano come omotetrameri, cioè
sono formate da quattro subunutà, ciascuna delle quali può
legarsi ad una molecola di CO2, al NADPH (un cofattore riducente) e
ad una molecola di substrato (enoil-CoA). Durante la fissazione del
carbonio, uno ione idruro (H-) viene trasferito dal NADPH alla
molecola di substrato. Questo passaggio rende il substrato altamente
reattivo, permettendogli di reagire con l'anidride carbonica legata
per formare un nuovo prodotto (un estere alchil-CoA).
Sincronizzazione enzimatica
Come si spiega l'impressionante velocità ed efficienza delle
ECR nella fissazione del carbonio? Recenti studi hanno scoperto un meccanismo
di sincronizzazione unico che facilita la catalisi rapida. L'ECR tetramerico
adotta una configurazione a "coppia di dimeri", in cui ciascuna
subunità forma un dimero con la subunità vicina, e i due
dimeri si assemblano in una geometria a forma di "X". Questa
speciale disposizione consente un'azione coordinata durante il ciclo
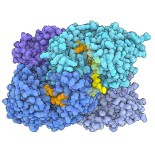
catalitico. Nello stato iniziale vuoto (PDB 6NA3),
l'enzima è simmetrico, ma dopo il legame con NADPH (mostrato
in arancione qui sotto), il tetramero subisce un cambiamento conformazionale
(PDB 6NA6). Una subunità di ciascun
dimero si chiude in modo coordinato, posizionando con precisione il
substrato (mostrato in giallo), NADPH e l'anidride carbonica (non mostrata)
in stretta prossimità per la fissazione del carbonio (PDB 6NA4).
Una volta che la reazione è completa, le subunità si riaprono
per rilasciare il prodotto. Questo evento di rilascio innesca la chiusura
della subunità partner all'interno del dimero, iniziando il successivo
ciclo di catalisi.
La commutazione sincronizzata tra stati aperti e chiusi è accoppiata
a un movimento di torsione del complesso enzimatico, che si pensa migliori
il legame del substrato e/o il rilascio del prodotto. Si ritiene che
la rapida e accoppiata sincronizzazione delle subunità dell'ECR
sia un fattore chiave che contribuisce a prestazioni superiori rispetto
alla Rubisco.
 Esplorando
la struttura Esplorando
la struttura
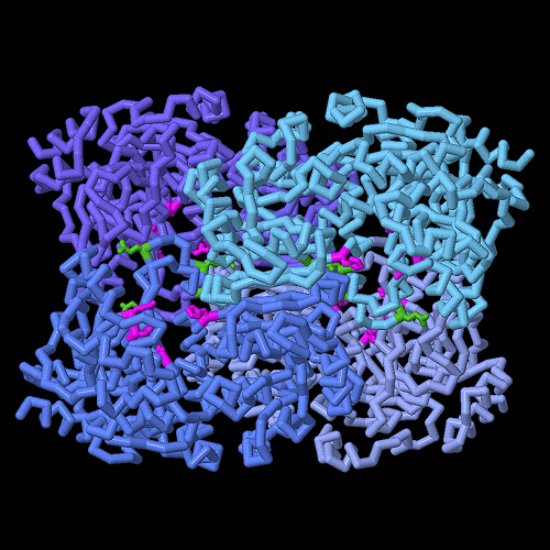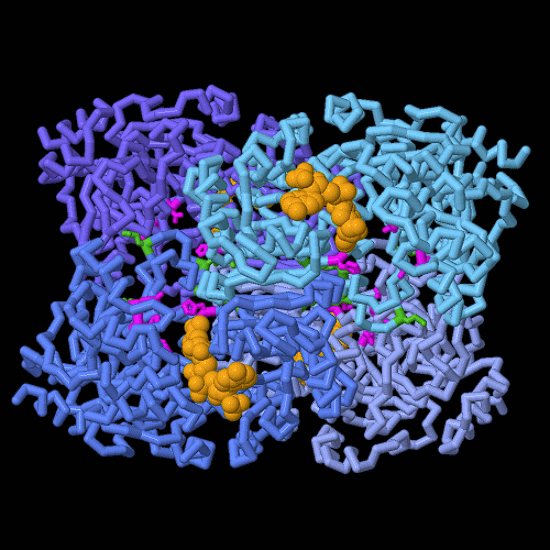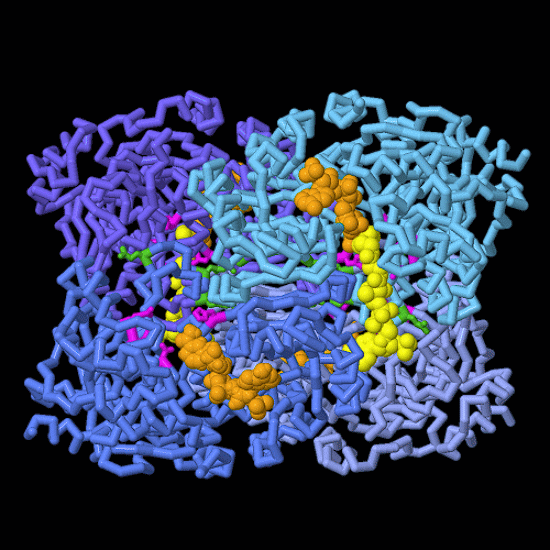
Uno sguardo più da vicino alla fissazione del carbonio.
Nell'immagine qui a fianco, si vedono, in sequenza, le strutture delle
tre diverse conformazioni di ECR discusse sopra (vuota, con NADPH, e
con NADPH più substrato enoil-CoA).
Sono evidenziati in magenta gli amminoacidi
coinvolti nel legame dell'anidride carbonica e in verde quelli coinvolti
nel coordinamento della sincronizzazione enzimatica.
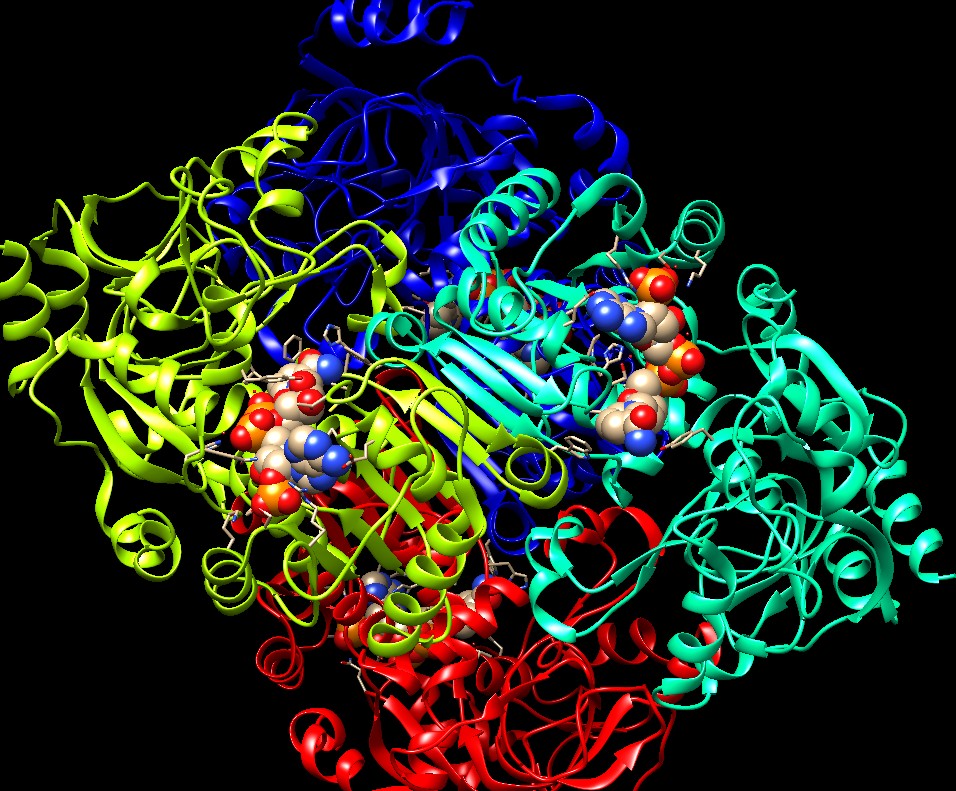
Nella figura qui sotto è mostrato l'enzima ECR legato al NADPH
(PDB 6NA6) rappresentato con Chimera (un
programma freeware di modellistica molecolare).
. . 
Spunti per ulteriori esplorazioni
La Rubisco, considerata uno degli enzimi più abbondanti del pianeta,
è utilizzata da piante e alghe per fissare l'anidride carbonica.
I cianobatteri utilizzano anche la Rubisco, immagazzinando più
copie dell'enzima in un organello chiamato carbossisoma
(mdm 9-2024): qui puoi leggere di più su questo e altri meccanismi
di cattura del carbonio
Questo studio ha sfruttato tecniche di cristallografia time-resolved,
che sono state utilizzate anche per studiare altri enzimi che catalizzano
rapidamente le reazioni, compresi gli studi sulle proteine
attivabili dalla luce (mdm 3/2017).
 Bibliografia Bibliografia
6OWE: Stoffel GMM, Saez DA, DeMirci H, Vögeli B, Rao Y,
Zarzycki J, Yoshikuni Y, Wakatsuki S, Vöhringer-Martinez E, Erb
TJ. (2019) Four amino acids define the CO2 binding pocket of enoyl-CoA
carboxylases/reductases. Proc Natl Acad Sci U S A. 2019 Jul 9;116(28):13964-13969.
6NA3, 6NA4, 6NA5, 6NA6: DeMirci H, Rao Y, Stoffel GM, Vögeli
B, Schell K, Gomez A, Batyuk A, Gati C, Sierra RG, Hunter MS, Dao EH,
Ciftci HI, Hayes B, Poitevin F, Li PN, Kaur M, Tono K, Saez DA, Deutsch
S, Yoshikuni Y, Grubmüller H, Erb TJ, Vöhringer-Martinez E,
Wakatsuki S. (2022) Intersubunit Coupling Enables Fast CO2-Fixation
by Reductive Carboxylases. ACS Cent Sci. 2022 Aug 24;8(8):1091-1101.
Schwander T, Schada von Borzyskowski L, Burgener S, Cortina NS,
Erb TJ.(2016) A synthetic pathway for the fixation of carbon dioxide
in vitro. Science. Nov 18;354(6314):900-904.
|
|
|