|
|
HER2, Trastuzumab e |
|||||
|
Molecola del mese di aprile 2022 Gli anticorpi monoclonali come Trastuzumab che colpiscono i recettori HER2 sono la nuova frontiera del trattamento del cancro al seno. 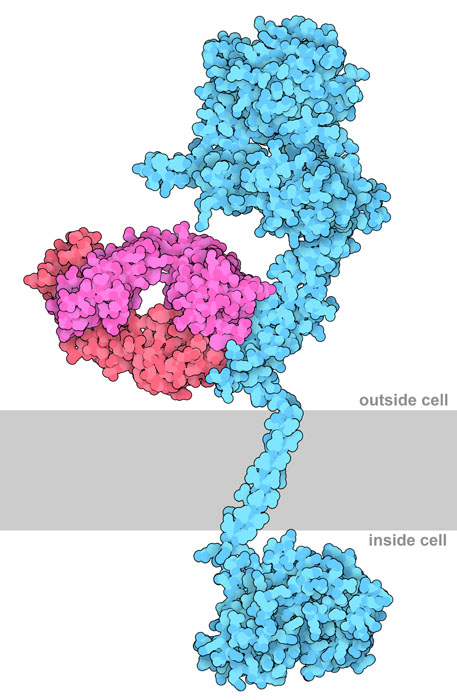 Introduzione IntroduzioneIl cancro al seno è la principale causa di morte per cancro nelle donne di tutto il mondo. Circa il 20% dei casi di cancro invasivo del seno presentano un eccessiva quantità di recettore 2 del fattore di crescita epiteliale umano (HER2), conosciuto anche col nome di ErbB2. Questo accade perchè il gene che codifica per HER2 fa molte copie di sè stesso e questo porta ad una sovraproduzione dei recettori HER2. Le pazienti con cancro al seno con un'eccessiva quantità di recettore HER2 hanno una minore aspettativa di vita e una risposta più bassa alla chemioterapia e al trattamento ormonale a causa di una crescita e una proliferazione incontrollata delle cellule cancerose. Capire il meccanismo di azione e la struttura tridimensionale di HER2 sta aiutando gli scienziati a scoprire nuove e più efficaci cure per il cancro al seno. Uno strano recettore HER2 appartiene ad una famiglia di 4 recettori tirosina-chinasi (HER1, HER2, HER3, HER4) che si trovano inseriti nella membrana di molte cellule in tutto il corpo. Questi recettori normalmente regolano importanti processi biologici come la crescita e la proliferazione cellulare, il metabolismo e la differenziazione. I recettori HER esistono in due conformazioni: chiusa e aperta. Nella forma chiusa, la proteina è piegata su sè stessa ed è incapace di accoppiarsi con un altro recettore. La forma aperta del recettore si ottiene in seguito all'interazione con un opportuno legando, solo nella forma aperta il recettore è in grado di formare dimeri e di dare inizio al processo di segnalazione. Il recettore HER2 è diverso dagli altri di questa classe perchè si trova sempre nella forma aperta e non richiede l'intervento di un legando per legarsi ad un altro recettore e formare il dimero attivo. Nel normale processo di segnalazione, HER2 forma dimeri con altri recettori HER. Nelle cellule cancerose, però, la grande concentrazione di HER2 favorisce anche la formazione di dimeri tra due recettori uguali HER2 (omodimeri) e questo stimola con più forza la cellula a riprodursi. Colpire HER2 La comprensione della struttura di HER2 sta aiutando a mettere a punto nuove e più efficaci terapie contro il cancro al seno. Trastuzumab è un anticorpo monoclonale creato in laboratorio ed è stato approvato dalla FDA (Food and Drug Administration) per la terapia anti-HER2 del cancro al seno. Trastuzumab si lega al recettore HER2 bloccando la formazione di omodimeri e così inibisce la proliferazione delle cellule rallentando la crescita del cancro al seno dipendente da HER2. La figura qui sopra è stata creata usando tre diverse stutture PDB. Il dominio extracellulare legato alla porzione Fab di Trastuzumab (Fab: antigen binding Fragment, rossa e magenta) è preso dal file PDB 1n8z. Il dominio transmembrana è preso dal file PDB 2ks1, Il dominio chinasi interno alla cellula è preso dal file PDB 3pp0. Sfortunatamente, dopo una buona risposta clinica iniziale, l'efficacia dell'anticorpo dimunuisce a causa della resistenza che spesso si manifesta dopo le prime somministrazioni di Trastuzumab.  Contrastare
la resistenza Contrastare
la resistenzaTrastuzumab ha notevolmente migliorato la prognosi delle pazienti di cancro del seno positivo a HER2. Comunque circa il 50-60% delle pazienti diventa resistente e non risponde più all'anticorpo. Gli scienziati hanno contrastato questa resistenza con il Pertuzumab, un nuovo anticorpo che colpisce lo stesso recettore HER2, ma in modo diverso. Come si vede nelle struttura PDB 1s78 qui a fianco, questo anticorpo si lega al recettore in un punto più lontano dalla membrana, bloccando un sito che HER2 usa per formare il dimero con un altro recettore HER. In particolare Pertuzumab impedisce la formazione di dimeri HER2-HER3 che hanno un ruolo chiave nello sviluppo del cancro. Anche Pertuzumab è stato approvato dalla FDA e, bloccando la cascata di segnali innescata dall'attività di chinasi del recettore, ha contribuito a migliorare ulteriormente le percentuali di guarigione nelle pazienti che non rispondevano più al trattamento. Esplorando la struttura HER2 legato a Pertuzumab e Trastuzumab  La
disponibilità di due diversi anticorpi per la cura del cancro al
seno si è dimostrata un grande vantaggio. Usando una combinazione
di Trastuzumab e Pertuzumab, conosciuta come Doppia inibizione di HER2,
si riesce a superare la resistenza al Trastuzumab. Quando il recettore
HER2 è legato agli anticorpi in due diverse posizioni (come si
vede nel file PDB 6oge qui a fianco) è
più difficile per la proteina mutare e diventare resistente ad
entrambi i farmaci nello stesso tempo. Inoltre questa combinazione aiuta
a colpire molti degli elementi funzionali di HER2 che provocavano la progressione
del cancro. Trastuzumab blocca la formazione di omodimeri HER2-HER2, ma
lascia libero il dominio di HER2 che forma eterodimeri. D'altra parte
Pertuzumab ha la capacità di impedire la formazione di eterodimeri
HER2-HER3. La combinazione dei due farmaci ottiene i benefici di entrambi.
Il trattamento di Doppia inibizione di HER2 ha dimostrato di migliorare
in modo significativo la sopravvivenza delle pazienti rispetto alla cura
con un singolo farmaco. La
disponibilità di due diversi anticorpi per la cura del cancro al
seno si è dimostrata un grande vantaggio. Usando una combinazione
di Trastuzumab e Pertuzumab, conosciuta come Doppia inibizione di HER2,
si riesce a superare la resistenza al Trastuzumab. Quando il recettore
HER2 è legato agli anticorpi in due diverse posizioni (come si
vede nel file PDB 6oge qui a fianco) è
più difficile per la proteina mutare e diventare resistente ad
entrambi i farmaci nello stesso tempo. Inoltre questa combinazione aiuta
a colpire molti degli elementi funzionali di HER2 che provocavano la progressione
del cancro. Trastuzumab blocca la formazione di omodimeri HER2-HER2, ma
lascia libero il dominio di HER2 che forma eterodimeri. D'altra parte
Pertuzumab ha la capacità di impedire la formazione di eterodimeri
HER2-HER3. La combinazione dei due farmaci ottiene i benefici di entrambi.
Il trattamento di Doppia inibizione di HER2 ha dimostrato di migliorare
in modo significativo la sopravvivenza delle pazienti rispetto alla cura
con un singolo farmaco.Spunti per ulteriori esplorazioni Molti recettori di membrana trasmettono il loro segnale all'interno della cellula tramite la formazione di dimeri. Per trovare altri esempi di questo meccanismo, consultate le molecole del mese Ormone della crescita (mdm 4-2004), Fattori di crescita epiteliale (EGF) (mdm 6-2010), Fattore di crescita dell'endotelio vascolare (VegF) (mdm 3-2022). Il Trastuzumab è stato anche legato chimicamente a farmaci che colpiscono altre molecole, come il farmaco maytansina che si lega ai microtubuli (file PDB 4tv8). Nel farmaco composito, Trastuzumab si lega alla cellula cancerosa e la maytansina la uccide destabilizzandone i microtubuli. 6oge: Hao Y., Yu X., Bai Y., McBride H.J., Huang X. (2019) Cryo-EM Structure of HER2-trastuzumab-pertuzumab complex. PLoS One. 14(5):e0216095. Ling W.L., Lua W.H., Poh J.J., Yeo J.Y., Lane D.P., Gan S.K. (2018) Effect of VH-VL Families in Pertuzumab and Trastuzumab Recombinant Production, Her2 and FcgIIA Binding. Front Immunol. 9:469. Roskoski R.Jr. (2014) The ErbB/HER family of protein-tyrosine kinases and cancer. Pharmacol Res. 79:34-74. Olson E.M. (2012) Maximizing human epidermal growth factor receptor 2 inhibition: a new oncologic paradigm in the era of targeted therapy. J Clin Oncol. 30(14):1712-4. 3pp0: Aertgeerts K., Skene R., Yano J., Sang B.C., Zou H., Snell G., Jennings A., Iwamoto K., Habuka N., Hirokawa A., Ishikawa T., Tanaka T., Miki H., Ohta Y., Sogabe S. (2011) Structural analysis of the mechanism of inhibition and allosteric activation of the kinase domain of HER2 protein. J Biol Chem. 286(21):18756-65. Hanahan D., Weinberg R.A. (2011) Hallmarks of cancer: the next generation. Cell. 144(5):646-74. LoRusso PM., Weiss D., Guardino E., Girish S., Sliwkowski MX. Trastuzumab emtansine: a unique antibody-drug conjugate in development for human epidermal growth factor receptor 2-positive cancer. (2011) Clin Cancer Res. 17(20):6437-47. 2ks1: Mineev K.S., Bocharov E.V., Pustovalova Y.E., Bocharova O.V., Chupin V.V., Arseniev A.S. (2010) Spatial structure of the transmembrane domain heterodimer of ErbB1 and ErbB2 receptor tyrosine kinases. J Mol Biol. 400(2):231-43. Hudis C.A. (2007) Trastuzumab--mechanism of action and use in clinical practice. N Engl J Med. 357:39-51. 1s78: Franklin M.C., Carey K.D., Vajdos F.F., Leahy D.J., de Vos A.M., Sliwkowski M.X. (2004) Insights into ErbB signaling from the structure of the ErbB2-pertuzumab complex. Cancer Cell. 5(4):317-28. 1n8z: Cho H.S., Mason K., Ramyar K.X., Stanley A.M., Gabelli S.B., Denney D.W. Jr., Leahy D.J. (2003) Structure of the extracellular region of HER2 alone and in complex with the Herceptin Fab. Nature. 421(6924):756-60. |
||||||
|
|
||||||
