|
|
Adenilil ciclasi |
|||||
|
Molecola del mese di novembre 2020 L'enzima adenilil ciclasi crea dei messaggeri secondari per amplificare il segnale dei recettori accoppiati alla proteina G. 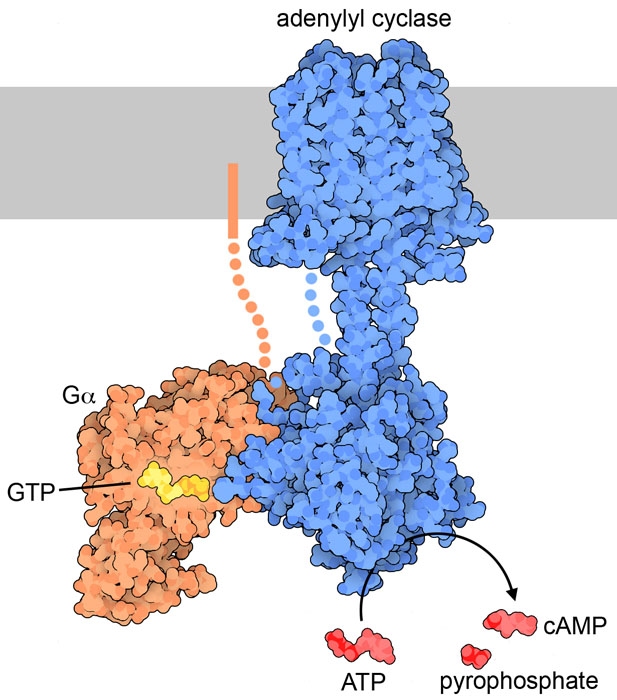 Introduzione IntroduzioneL'adenilil ciclasi è un amplificatore di segnale. Agisce nel cuore della cascata di segnalazione che trasforma il legame con un ormone sulla superficie cellulare in una risposta della cellula. Quando ormoni come l'adrenalina (mdm 4-2008) o il glucagone (mdm 4-2015) si legano ad un recettore di membrana accoppiato ad una proteina G (mdm 10-2004), questa si attiva, si sposta, e va ad attivare l'adenilil ciclasi. Questo è un enzima che crea un nuovo anello nell'ATP unendo l'OH in posizione 3' con il fosfato in posizione 5' grazie all'espulsione degli ultimi due fosfati dell'ATP. La molecola risultante, AMP ciclico o cAMP, è rilasciata nel citoplasma e arriva velocemente in ogni punto della cellula regolando la funzione di molte proteine. In questo ruolo, cAMP è chiamato messaggero secondario perché trasporta all'interno della cellula il segnale dell'ormone, il messaggero originale. Il segnale, inoltre, non è solo trasmesso, ma è anche amplificato perché l'adenilil cilclasi è un enzima che può formare molte molecole di cAMP quando la proteina G è attivata da una molecola di ormone. Complesso di segnalazione La segnalazione mediata da cAMP è importante in molti processi come il bilanciamento tra la rottura e la sintesi di zuccheri nella produzione di energia, nel controllo della crescita cellulare, dell'apprendimento e della memoria. Per regolare tutti questi processi vi sono dieci diversi sottotipi di adenilil ciclasi. Nove di questi hanno una struttura simile con una porzione che attraversa la membrana e un dominio catalitico sul lato rivolto verso il citoplasma. Nella figura qui a fianco (file PDB 6r3q) è mostrato il sottotipo AC9 che si trova nei polmoni, nel cervello, nel cuore e in altri tessuti. Questa struttura, ottenuta con la microscopia crioelettronica, contiene anche la proteina G (arancione) legata al dominio citoplasmatico della adenilil ciclasi e ci mostra il complesso di segnalazione nel pieno della sua azione. Messaggeri secondari I messaggeri secondari sono talmente importanti che si trovano nella maggior parte degli organismi. Nei batteri, l'AMP ciclico, prodotto dall'adenilil ciclasi quando il glucosio è carente, si lega alla proteina CAP attivatrice dei geni dei cataboliti (mdm 12-2003) e la induce a legarsi al DNA dove attiva l'operone lac (mdm 3-2003) per la degradazione del lattosio. Nelle nostre cellule vi è anche una adenilil ciclasi solubile (non mostrata, file PDB 4clk), molto diversa dalle altre nove che sono tutte trans-membrana, che è coinvolta nel rilevare i livelli di bicarbonato e di anidride carbonica. Talvolta questi enzimi sono usati per offendere. Per esempio, il batterio dell'antrace forma una proteina che induce l'edema, agendo come una adenilil ciclasi, altera le segnalazioni degli organismi infettati.  Attivare
i canali ionici Attivare
i canali ioniciIl cAMP ha una funzione regolatrice su molte proteine. Per esempio la PKA (proteina chinasi cAMP dipendente) (mdm 8-2012) quando è attivata da cAMP inizia a fosforilare le proteine che controllano l'utilizzo dell'energia. HCN1 (canale ionico attivato dalla iperpolarizzazione) è un canale ionico controllato dal voltaggio che fa entrare o uscire ioni dalle cellule del cuore e dei neuroni che controllano il battito cardiaco. La struttura di HCN1 mostrata qui a fianco (file PDB 5u6p) ha un cAMP legato in ognuna delle 4 subunità identiche che formano il canale ionico. Il legame con cAMP aumenta l'attività del canale e fa accelerare il battito cardiaco. Esplorando la struttura Le prime strutture di adenilil ciclasi che sono state determinate contenevano solo il dominio catalitico perché le proteine di membrana sono apolari e quindi sono difficili da sciogliere in acqua e cristallizzare.  Nella
struttura mostrata qui a fianco (file PDB 1cjk)
si vede la proteina G attivata (contiene GTP) che introduce la sua alfa
elica di segnalazione (rossa) in una tasca sul fianco della adenilil ciclasi.
Il dominio catalitico della adenilil ciclasi è formato da due catene
molto simili (azzurra e blu) che contengono due tasche vicine tra loro. Nella
struttura mostrata qui a fianco (file PDB 1cjk)
si vede la proteina G attivata (contiene GTP) che introduce la sua alfa
elica di segnalazione (rossa) in una tasca sul fianco della adenilil ciclasi.
Il dominio catalitico della adenilil ciclasi è formato da due catene
molto simili (azzurra e blu) che contengono due tasche vicine tra loro.
Una di queste lega ATP e realizza la reazione di ciclizzazione (in questa struttura vi è una forma modificata di ATP che non può ciclizzare). La seconda tasca ha una funzione regolatoria e contiene forskolina una molecola stimolatrice vegetale. Il sito catalitico trasferisce il gruppo fosfato 5' sull'OH 3' con l'aiuto di due ioni magnesio con un meccanismo simile a quello della DNA polimerasi. I loro siti attivi sono così simili che si pensa che i due enzimi derivino da un precursore comune. Spunti per ulteriori esplorazioni Cercate "cAMP" nel sito RCSB per trovare le strutture di molte delle proteine regolate da cAMP. Esplorate la struttura di cAMP nella "Chemical Component Library" di CMP.  Bibliografia Bibliografia6r3q: Qi, C., Sorrentino, S., Medalia, O., Korkhov, V.M. (2019) The structure of a membrane adenylyl cyclase bound to an activated stimulatory G protein. Science 364: 389-394 Halls, M. L., Cooper, D. M. F. (2017) Adenylyl cyclase signalling complexes - pharmacological challenges and opportunities. Pharmacology & Therapeutics 172, 171-180. 5u6p: Lee, C.H., MacKinnon, R. (2017) Structures of the Human HCN1 Hyperpolarization-Activated Channel. Cell 168: 111-120.e11 4clk: Kleinboelting, S., Diaz, A., Moniot, S., Van Den Heuvel, J., Weyand, M., Levin, L.R., Buck, J., Steegborn, C. (2014) Crystal Structures of Human Soluble Adenylyl Cyclase Reveal Mechanisms of Catalysis and of its Activation Through Bicarbonate. Proc Natl Acad Sci USA 111: 3727 1cjk: Tesmer, J.J., Sunahara, R.K., Johnson, R.A., Gosselin, G., Gilman, A.G., Sprang, S.R. (1999) Two-metal-Ion catalysis in adenylyl cyclase. Science 285: 756-760.
|
||||||
|
|
||||||
